Coût sanitaire de l’énergie
- Publié le 23 novembre 2017
Le coût sanitaire associé au réchauffement climatique et à l’épuisement des ressources est une composante majeure du coût externe de l’énergie ….
télécharger ce document en pdf
1 - Introduction
L’impact sanitaire de la production et de la consommation d’énergie participe pour une part déterminante au coût externe de l’énergie, c’est-à-dire au prix non payé par les acteurs du marché de l’énergie mais payé par la société dans son ensemble.
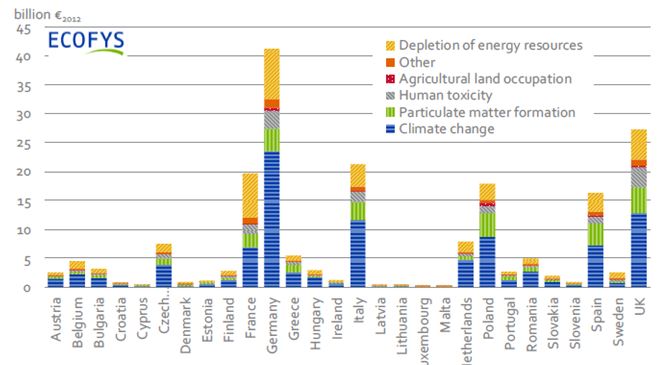
Dans la dernière analyse européenne[1] qui met à jour le bilan de l’étude ExternE lancée dans les années 1990, l’évaluation monétaire de l’impact sanitaire est situé au 3ème rang, après celui imputé au changement climatique et celui constitué par l’épuisement des ressources : fig 1.
Figure 1 Coût monétaire externe de l’énergie en Europe. Les impacts sanitaires apparaissent sous les appellations ‘’human toxicity’’ et ‘’Particulate matter formation’’ composant majeur de la pollution de l’air, et dans une fraction des coûts de ’’climate change’’ affectée à quelques conséquences identifiées et chiffrables du réchauffement climatique sur la santé.
Les coûts de l'impact sanitaire sont cependant susceptibles d’être revu à la hausse, compte tenu des incertitudes sur le coût des pathologies émergentes associées au réchauffement climatique non comptabilisées, et de l’évaluation monétaire sans cesse croissante du coût de la vie humaine.
Par ailleurs l’impact sanitaire a la particularité d’introduire dans l’analyse une dimension éthique importante, car si les bénéfices de l’énergie valent pour l’ensemble de la communauté, les conséquences médicales de l’impact de l’énergie ne sont supportées que par les victimes. La mutualisation du coût sanitaire, calculée sur la perte moyenne d’espérance de vie, fait implicitement l’hypothèse d’une répartition équitable du fardeau sanitaire ce qui est loin d’être vraisemblable si on prend en compte l’existence avérée de groupes à risque et l’inéquitable survenue des maladies chroniques comme le cancer. Cette considération est importante car elle influence directement une acceptabilité des risques difficile à faire admettre sur la simple base de l’optimisation des coûts.
2 - Identification des risques
L’identification des dommages sanitaires imputables à l’énergie doit prendre en compte l’ensemble du cycle de vie de chaque filière et de chacun de ses constituants. Ceci inclut, dans les situations accidentelles et en fonctionnement normal, les impacts de l’extraction, de la transformation, de la production, du transport et des déchets.
2-1 Impact des accidents
La production d’énergie comporte des nuisances affectées à l’ensemble du cycle de vie. En premier lieu par la survenue d’accidents sévères affectant les professionnels et le public. 442 de ces accidents ont été relevés dans les pays de l’OCDE, de 1970 à 2008, aboutissant à près de 8.900 décès accidentels imputables dans l’ordre aux filières du pétrole, du gaz et du charbon. Hors OCDE ce sont plus de 2.900 accidents qui provoqué plus de 90.000 décès accidentels attribuables au charbon, à l’hydro électricité au pétrole et au gaz. Trois accidents ont affecté les centrales nucléaires dont seul celui de Tchernobyl a provoqué les décès accidentels de 31 victimes irradiées à dose létale.
Les décès qui suivent immédiatement l’accident ne sont bien répertoriés que dans le cas des accidents majeurs qui affectent les barrages hydrauliques, le transport et le stockage des dérivés pétroliers, le nucléaire et les accidents dans les mines de charbon, par contre, il est difficile de faire la part des victimes attribsuables aux filières décentralisées : éolienne, photovoltaïque et biomasse.
Dans le cas du nucléaire on ajoute aux décès immédiats ou très précoces les décès différés par cancer et, éventuellement d’autres maladies, qui peuvent être la conséquence tardive de surexpositions accidentelles aux rayonnements ionisants parmi les professionnels et le public ; l’évaluation en est faite par modélisation et il y a débat sur la validité du modèle dans le cas des très faibles expositions ; la somme des décès par cancer après Tchernobyl peut ainsi varier de 4000 à 30.000 selon que l’on applique le modèle uniquement ou non aux expositions supérieures à 100 mSv, dose au dessous de laquelle l’épidémiologie est muette.
Les conséquences tardives sur la santé humaine des contaminations de l’environnement imputables aux accidents dans les filières autres que nucléaire ne sont par contre pas prises en compte.
Enfin les effets collatéraux générés par les accidents désorganisant le cadre de vie par les évacuations constituent un important facteur d’anxiété dont les conséquences sur la santé demanderaient à être individualisées avec rigueur. L’expérience Tchernobyl et de Fukushima montrent que leurs conséquences peuvent surpasser celles des effets directs des accidents.
Un million de résidents ont été déplacés par les accidents non nucléaires.
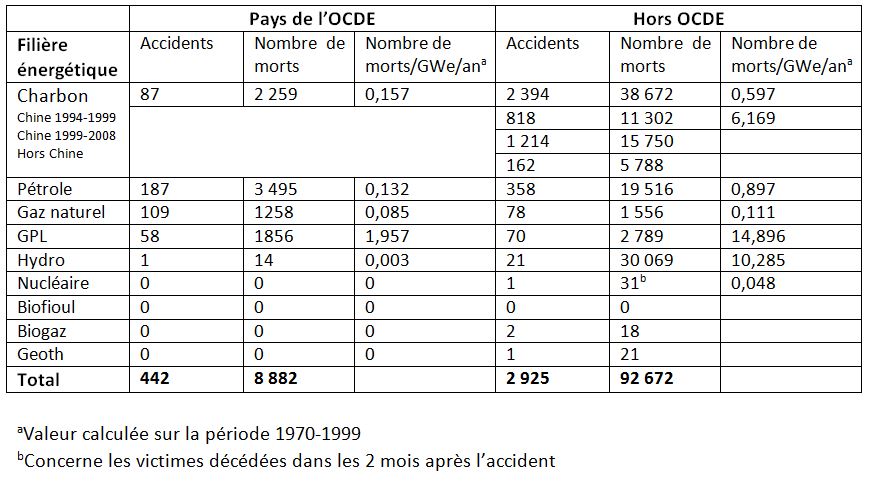
Les conséquences des accidents sont bien connues, pour les plus graves d’entre eux, depuis l’étude ENSAD (ENergy-related Severe Accident Database) conduite par l’institut Paul Scherrer en 1998[2]. Ces estimations ont été revues en 2014 et couvrent désormais la période 1970-2008[3]
Tableau 1 : Nombre d’accidents sévères et de décès précoces attribuables aux filières de l’énergie[4] : charbon, pétrole, gaz naturel, gaz de pétrole liquéfié, hydroélectricité, nucléaire. Les accidents sévères sont ceux qui impliquent l’un des critères suivants : au moins 5 décès, ou au moins 200 évacués, ou l’interdiction de consommation des produits locaux, ou le rejet de plus de 10.000 tonnes d’hydrocarbures etc…
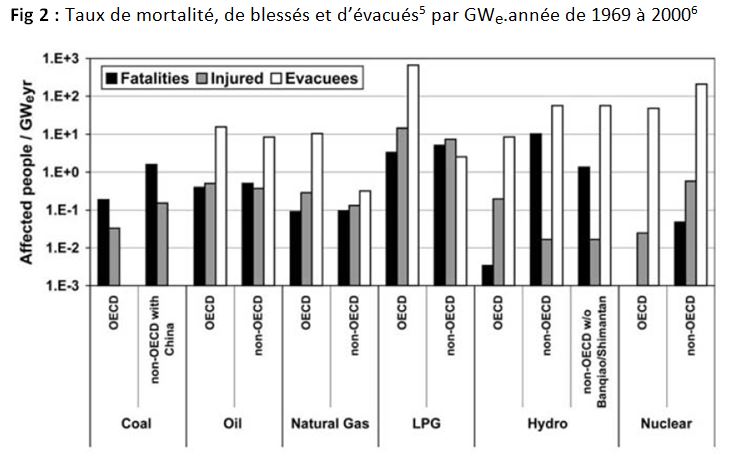
Après normalisation en fonction de la production électrique, et en introduisant dans l’évaluation les cas de blessures invalidantes et le nombre d’évacués la comparaison des différentes énergies apparaît pour la même période dans la figure 2 :
Concernant la répartition des accidents (ENSAD) ils interviennent : pour le charbon à l’extraction minière pour 96% ; pour le pétrole pour 76% au transport et au stockage, 15% au forage et 8% au raffinage ; pour le gaz naturel à 78% au transport et au stockage, 6% au forage, et 5% à la production ; pour le nucléaire entièrement à la production.
Les décès tardifs imputables aux expositions environnementales accidentelles aux dérivés des produits pétroliers et de la biomasse ne sont pas comptabilisés.
Dans le cas du nucléaire la très grande majorité des décès provient par extrapolation de l’évaluation des cancers radioinduits[7] qui pourraient apparaître jusqu’à 50 années après l’exposition. Ces cancers ne peuvent actuellement être distingués de ceux intervenant pour d’autres causes dans les populations exposées. Pour les expositions supérieures à 100 mSv, les données épidémiologiques des survivants de Hiroshima et Nagasaki servent de référence pour l’évaluation de risque.
Pour ce qui concerne les expositions inférieures à 100 mSv aucune donnée n’établit qu’un risque existe proportionnellement à la dose reçue ; par précaution on admet cependant qu’il n’est pas actuellement possible d’exclure l’existence d’un tel risque.
Selon que l’on considère que cette hypothèse vaut pour l’ensemble des populations du monde, aussi faibles que soient les doses reçues, ou que l’on souhaite restreindre le calcul à des populations dont les doses engagées ne s’écartent pas de plusieurs ordres de grandeur de 100 mSv, le décompte des décès attribuables varie de manière importante. Ainsi dans le calcul de l’Institut Paul Scherrer la fourchette proposée est comprise entre 9.000 et 33.000[8] décès à intervenant en majorité en fin de vie tous imputables à l’accident de Tchernobyl. Avec la même hypothèse, l’accident de TMI aboutirait à 1 décès attribuable.
Pour les liquidateurs de 1986-87 de Tchernobyl exposés à plus de 150 mSv (Unscear 2008[9]) restreindre aux cancers radioinduits le nombre de décès imputables est une sous évaluation : il faut également prendre en compte un excès de mortalité attribuable aux effets cardio vasculaires radioinduits dont le poids sanitaire est voisin de celui des cancers. Ces effets n’apparaissent qu’au-delà d’un seuil de dose supérieur à la plupart des expositions environnementales accidentelles.
En dehors des effets directs de l’irradiation il faut prendre en compte les effets indirects qui résultent de la gestion de crise post accidentelle, notamment ceux qui sont imputables aux évacuations de territoire, environ 115.000 résidents dans la zone de Tchernobyl et 160.000 dans celle de Fukushima.
Cette composante a un coût sanitaire mais il est difficile à évaluer. Il peut néanmoins dépasser de beaucoup celui des effets sanitaires directement provoqués par l’accident lui-même. Dans le cas de l’accident de Fukushima, qui n’a fait aucune victime par exposition aux rayonnements ionisants, le déplacement des populations et leur relogement dans des conditions de fortune a conduit les autorités japonaises à reconnaître environ 2000 décès prématurés attribuables[10]. Le recensement de ces cas continue plus de 5 ans après l’évacuation. Les conséquences dramatiques immédiates de l’évacuation dans un pays dévasté par le tsunami du 11 mars 2011 n’expliquent que très partiellement cette prise en compte administrative. Ce sont les effets du stress post traumatique, le désespoir d’avoir dû quitter les lieux de vie, l’angoisse d’avoir été exposé à un danger insidieux, la difficulté à affronter un environnement social inconnu et éventuellement hostile qui sont à l’origine de troubles réels très divers avec un cortège important d’états dépressifs et de suicides[11].
Dans son évaluation du coût d’un accident nucléaire en France, comportant 100.000 évacués, la part de ces effets psychologiques est évaluée par l’IRSN entre 12 et 22 milliards d’euros[12]
C’est cette composante sanitaire du post accident qui est vraisemblablement le fardeau sanitaire le plus lourd de l’accident de Tchernobyl, celui qui est à l‘origine des évaluations les plus pessimistes comme celles publiées dans les Annales de l’Académie des sciences de New-York par les dissidents de l’ex URSS[13], concluant, mais sans support méthodologique évaluable, à un million de morts en excès. La prise en charge des populations précocément après l’accident de Tchernobyl n’a pas été faite comme elle l’avait été pour les déplacés de TMI, et comme elle l’a été pour les populations de Fukushima, de sorte qu’il ne sera jamais possible de faire le bilan exact de ces effets sanitaires indirects.
L’évaluation des conséquences sanitaires indirectes du post accident n’est faite que pour le nucléaire et n’apparaît que marginalement lors d’accidents de contamination environnementale par les dérivés du pétrole et du charbon où le coût des dommages à l’environnement domine. Elle devrait néanmoins être prise en compte, comme dans les situations de détérioration du cadre de vie associées aux industries extractives en fonctionnement normal ou dégradé (Bayan Obo pour les terres rares, Alberta pour l’extraction des sables bitumineux, Gazweiler pour le lignite, les Apalaches aux Etats Unis pour le charbon…) ou dans le cas de déplacement de populations pour la mise en eau de grands barrages (Barrage des Trois Gorges : 1,4 million de personnes déplacées selon Wikipedia).
2-2 Impact en fonctionnement normal.
2-2-1 Energie nucléaire
Les professionnels de l’énergie nucléaire sont suivis par dosimétrie et font régulièrement l’objet d’études épidémiologiques. Parmi ceux-ci les mineurs d’uranium exposés au radon ont développé plus de 10.000 cancers fatals depuis 1946, en très grande majorité dans l’ex RDA. Les autres personnels exposés ont une meilleure espérance de vie que la population générale. La comparaison des personnels les plus exposés par rapport aux moins exposés laisse néanmoins apparaître un excès de cancers et de leucémies attribuables à leur exposition de l’ordre de 0,1%. Sur la base d’une relation linéaire sans seuil on peut ainsi émettre l’hypothèse d’un excès de l’ordre de 300 cancers parmi les 300.000 travailleurs du nucléaire étudiés dans le monde en 2015.
Le public est exposé à de très faibles doses provenant des rejets des installations. Ces doses sont de l’ordre de 1% à 0,1% de la radioactivité naturelle ambiante. On ne peut établir de risques associés à ces très faibles niveaux de doses.
En fonctionnement normal comme dans les situations accidentelles la surexposition par voie externe ou interne aux rayonnements ionisants des professionnels et du public est le facteur essentiel de risque.
L’évaluation de l’exposition résulte de mesures et de modélisation. Pour le travailleur l’essentiel des doses accumulées, à l’exception des mineurs d’uranium exposés au radon, provient de l’exposition externe mesurée à titre individuel ou collectif ; pour le public l’essentiel de l’exposition est dû au relargage de différents radionucléides dans l’environnement et l’évaluation de dose se fait au travers de modélisation de leurs transferts dans l’air, l’eau et la chaîne alimentaire, à l’échelle locale, régionale et mondiale. Il en résulte une composante de dose externe et une composante interne dont la valeur est obtenue à partir de tables d’équivalence transformant les activités en becquerels inhalés ou ingérés en dose efficace. L’élaboration internationnale de ces tables a impliqué la connaissance du devenir biologique de chaque radionucléide et l’utilisation de facteurs de pondération tenant compte de la nature du rayonnement et du poids que représente chaque organe de rétention en matière de risque tardif.
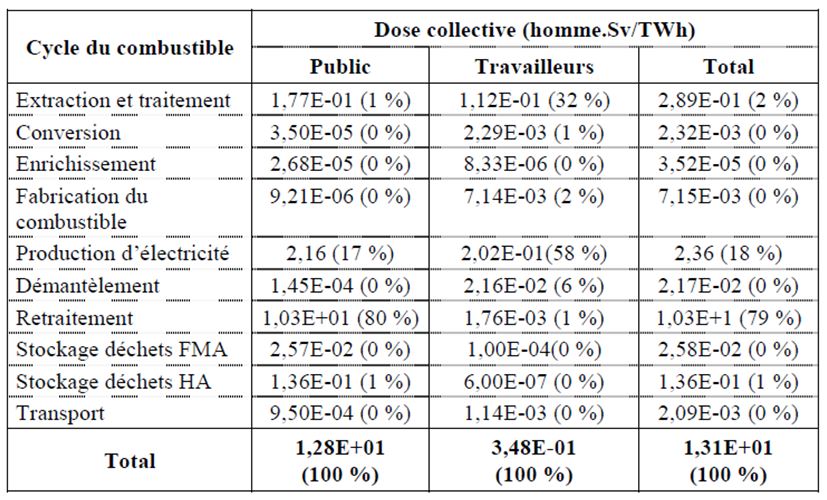
Tableau 2 : Doses collectives par TWh (somme des doses individuelles exprimées en hommes.sievert) au cours du cycle de combustible dans la filière nucléaire française (OCDE 2003[14])
Pour l’ensemble du cycle le bilan est de 13,1 homme.Sv par TWh calculés sur une période de 100.000 années. Si on restreint aux 100 premières années la dose collective peut être évaluée à 2,5 homme.Sv.
En appliquant ce modèle à l’ensemble de la production nucléaire mondiale et en répartissant l’ensemble des doses sur la population mondiale Rabl 2001[15] fait une estimation de dose par personne de 2,5 microsieverts par an. Avec une approche un peu différente l’UNSCEAR 2000[16] aboutit à une valeur 10 fois inférieure. Ce sont des niveaux de dose d’un ordre de grandeur 1000 fois inférieur à celui correspondant à la radioactivité naturelle dont l’impact sanitaire s’il existe ne peut qu’être inapparent.
Les groupes professionnellement exposés constituent un ensemble où un impact sanitaire de l’exposition aux rayonnements ionisants est détectable. C’est le cas chez les mineurs d’uranium exposés au radon. Plus de 10 000 d’entre eux sont morts de cancers du poumon depuis 1946 dont plus de 7000 en ex RDA[17], la plupart exposés à des niveaux extrêmement élevés. En France 211 mineurs sont morts de cancer du poumon sur 5000 mineurs exposés soit 1,43 fois la fréquence attendue dans la population masculine comparable non exposée[18]. Pour les autres travailleurs du nucléaire les études épidémiologiques font apparaître un déficit de cancers par rapport à la population générale, interprété comme effet du travailleur sain, sans que l’on sache exactement ce que ce concept rassemble en matière de protection contre les maladies cancéreuses. Il est néanmoins possible de faire apparaître un effet des expositions aux rayonnements ionisants chez les travailleurs du nucléaire en comparant entre eux les personnels affectés à différents niveaux de dose. Toujours avec l’hypothèse d’une relation dose effet à caractère linéaire sans seuil (INWORKS 2015)[19] la probabilité de mourir d’un cancer serait augmentée de 0,1% dans la population des 300 897 travailleurs suivis, soit environ 300 cancers en excès parmi les 75 000 attendus.
2-2-2 Energies carbonées
2-2-2-1 Extraction du charbon
L’extraction du charbon comporte de nombreux accidents du travail et expose les mineurs à la pneumoconiose (silicose) du mineur de charbon. Près de 100.000 mineurs en ont souffert en France et l’affection est encore de nos jours, en moyenne, à l’origine de 0,4 décès par 100.000 habitants par an dans les pays miniers. Les chiffres en Chine laissent apparaître 500.000 mineurs atteints de l’affection, avec 20.000 cas nouveaux par an.
En dehors des accidents l’extraction du charbon est à l’origine de maladies professionnelles dues à l’inhalation de poussières : pneumoconiose-silicose et cancer du poumon.
Les décès par silicose dans les mines de charbon en France, de 1946 à 1986 ont affecté 34.000 mineurs selon les statistiques des houillères, pour un effectif maximal de 330.000 mineurs en 1950 dont 2/3 de mineurs de fond, 20% d’entre eux ayant été reconnus atteints par la silicose. Ces chiffres sont probablement sous estimés et le nombre total de décès par silicose a été réévalué entre 80.000 et 120.000.[20]
Le nombre actuel de décès annuels par pneumoconiose du mineur de charbon est en moyenne de 0,4 pour 100.000 habitants dans le monde, dont en Allemagne environ 80[21] et 140 au Royaume Uni[22]
La prévalence des cas de pneumoconiose-silicose en Chine implique actuellement plus de 500 000 mineurs avec un nombre de cas nouveaux sans doute supérieur à 20.000 par an. Ces chiffres sont probablement très sous évalués et il faut y ajouter plus de 10.000 accidents du travail mortels par an[23]
2-2-2-1 Impact sanitaire du CO2
L’accumulation de CO2 provoquée dans l’atmosphère par les énergies carbonées réchauffe le climat et impacte sévèrement la santé humaine par de multiples voies.
Le potentiel d’émission pour le charbon et le lignite est de l’ordre de 350 g/KWh, pour le fioul de 280 g/KWh et de 200 g/KWh pour le gaz naturel (CITEPA Ominea). Pour la production d’électricité, ces valeurs sont de l’ordre de 1000 g pour l’ensemble charbon lignite, 900 g pour le fuel lourd, 750 g pour le diesel des groupes électrogènes , 450 g pour le gaz en centrale à cycle combiné gaz[24].
La production annuelle de CO2 en et France en 2014 était de 300 Mt dont la moitié environ provenant du fioul domestique, de l’essence et du gazole et gazole non routier (GNR), l’autre moitié était partagée entre industrie manufacturière, agriculture et transformation de l’énergie , compte non tenu de la part revenant à la biomasse (CITEPA-Secten 2016).
La production de CO2 constitue le facteur de risque commun à l’ensemble des énergies carbonées et contribue de façon déterminante au réchauffement climatique associé à de multiples effets sur la santé. Plus des ¾ des jours chauds depuis 1850 ont été attribués au réchauffement climatique et les canicules qui en ont résulté ont été à l’origine en France de plus de 20 000 décès prématurés. Il apparaît de plus, qu’en dehors des canicules, plus de 7% de la mortalité annuelle mondiale résulte des effets de la température et qu’il n’y a pas de bénéfice à attendre de la disparition des jours froids[25]. En outre le réchauffement climatique modifie l’aire de répartition des ressources agricoles et des ressources en eau, ce qui laisse prévoir d’importantes répercussions sanitaires difficiles à évaluer. Enfin le changement climatique a dès maintenant un impact sur l’évolution de la répartition d‘espèces végétales nuisibles, certaines à l’origine d’allergies sévères (ambroisie), et de la prolifération de vecteurs de maladies tropicales comme la dengue, le Chickungunya, le Zika dans les pays tempérés. Dans les pays tropicaux, l’évolution des diarrhées contagieuses est directement associée au réchauffement climatique de même que l’évolution de la malaria.
Le dioxyde de carbone est en outre un facteur aggravant de la pollution atmosphérique augmentant l’exposition à l’ozone et à divers cancérogènes organiques[26].
2-2-2-2 émissions toxiques
Au cours de leur combustion les sources carbonées d’énergie libèrent de nombreux toxiques à l’état gazeux et particulaire. Parmi les plus représentatifs figurent : - les gaz CO, NOx, SO2, et l’ozone formé secondairement par voie photochimique ; - les composés organiques volatils différents du méthane ; - la phase particulaire dans son ensemble ou scindée en différentes classes granulométriques en fonction du niveau de coupure granulométrique (PM10, PM2,5, nanoparticules…).
La composition des gaz et de la phase particulaire varie en fonction de la filière, charbon, fioul, biomasse et certains éléments métalliques ou organiques permettent d’en tracer l’origine.
Les différents constituants représentent plusieurs classes de danger, irritants locaux ou poisons systémiques, en particulier neurotoxiques, mutagènes et cancérogènes, cependant c’est essentiellement par l’action locale dans les voies respiratoires et les vaisseaux sanguins qu’ils vont exercer leur toxicité.
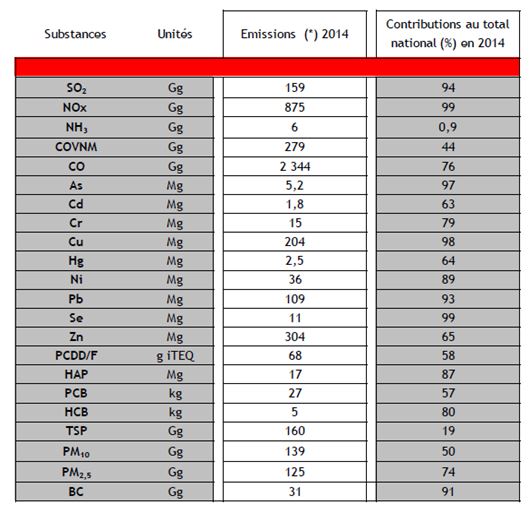
Le secteur de l’énergie en France, est à l’origine de rejets atmosphériques de divers composés toxiques dont les plus significatifs, rassemblées en 2016 par le CITEPA, apparaissent dans le tableau 3 où la dernière colonne donne la part respective du secteur de l’énergie dans l’ensemble des émissions nationales, tous secteurs confondus.
Glossaire
COVNM : composés organiques volatils différents du méthane (non méthane)
PCDD/F : polychlorobenzodioxines (PCDD) et les polychlorodibenzofuranes (PCDF) exprimés en équivalents toxiques à la dioxine de référence (TEQ)
HAP : hydrocarbures aromatiques polycycliques
PCB : polychlorobiphenyles
HCB : hexachlorobenzène
TSP : total des particules en suspension
PM10 : particules de diamètre inférieur à 10 micromètres
PM2,5 : particules de diamètre inférieur à 2,5 micromètres
BC : carbone
Tableau 3 Rejets toxiques
Les émissions ayant le plus fort impact sont les émissions particulaires : total particulaire (TSP), PM10, PM2,5 et carbone suie (BC) ; le CO, les oxydes d’azote (NOx) et composés organiques volatils différents du méthane (COVNM) en particulier responsables de la formation d’ozone par réaction photochimique, et SO2 toxique à l’état gazeux. S02 et NO2 sont en outre à l’origine d’un important contingent secondaire de particules atmosphériques par nucléation de sulfates et de nitrates après réaction avec des ions NH3 d’origine essentiellement rurale. Ces particules secondaires peuvent contribuer jusqu’à 80% de la masse des PM2,5 dans l’aérosol atmosphérique et servir de support à des éléments volatils de l’émission primaire.
Les autres constituants ont un potentiel de danger important notamment neurotoxique par les métaux Hg et Pb et cancérogène par les métaux (As, Cd, Ni, Cr) et par plusieurs composés organiques : hydrocarbures polycycliques aromatiques (HAP), dioxines et furanes (PCDD/F), hexachlorobenzène (HCB). Cependant les concentrations atteintes dans l’environnement général après dispersion sont faibles et ne modifient que marginalement le risque global. Ces toxiques peuvent cependant être à l’origine de la toxicité spécifique de certaines particules de l’aérosol atmosphérique inertes ou peu toxiques (nitrates) auxquelles ils s’associent. Il faut noter en outre que les métaux toxiques s’accumulent définitivement dans la biosphère après leur émission ; leur dépôt au sol,leur remise en suspension dans l’air et leur passage dans la chaîne alimentaire contribuent à un impact sanitaire potentiel sur plusieurs générations
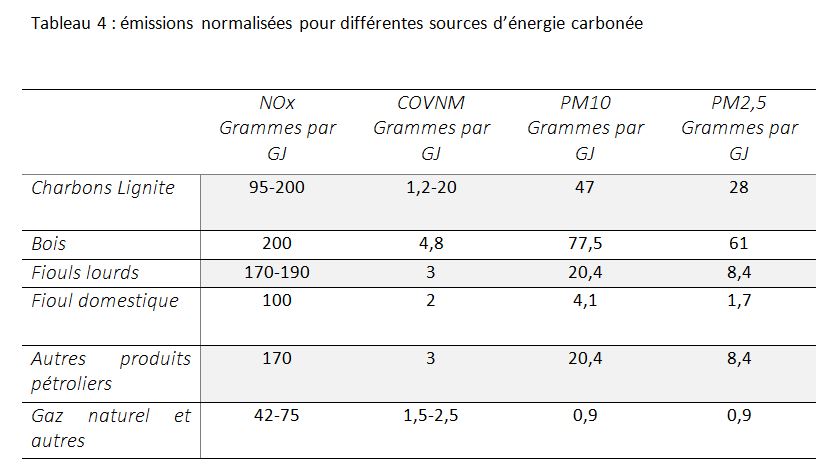
Les différentes sources d’énergie participent de manière variable à la dégradation de la qualité atmosphérique. Cette propriété est caractérisée par un facteur d’émission exprimant les grammes de polluants produits par unité de production d’énergie en GJ comme il apparaît dans le tableau 4 extrait de la publication CITEPA Ominea 92 pour les constituants principaux que sont les NOx, les COVNM les PM10 et les PM2,5.
Compte tenu des caractéristiques de l’utilisation de ces sources en France en 2014 (CITEPA Secten) l’ensemble des données fait apparaître comme sources principales d’émission par les moteurs et les chaudières : pour les NOx le gazole pour 65% des émissions ; pour les COVNM, le bois pour 52% des émissions, alors que le gazole et l’essence contribuent pour 32% ; pour les PM10 et les PM2,5 le bois pour environ 70% des émissions alors que le gazole et les fiouls y contribuent pour environ 30% (l’essence pour environ 2%). Pour le SO2 le charbon et les cokes contribuent à plus de 50% alors que les fiouls ne représentent plus que 13% des émissions en France.
Pour ce qui concernent les éléments As, Cr, Cu et Pb de l’aérosol atmosphérique la source principale est constituée par la combustion du bois et de la biomasse, reflétant un cycle court depuis les sols pollués. Pour le cadmium, les huiles et solvants constituent la source la plus importante suivie du bois et du charbon. Le mercure provient en majorité du charbon ; le nickel est un marqueur des produits pétroliers notamment des fiouls lourds.
Parmi les composés organiques toxiques : les dioxines et furanes proviennent de la combustion des déchets pour environ 50% des émissions suivies par le gazole 25%, le bois 15% et le charbon 13%. ; les HAP sont en majorité émis par le bois pour plus de 50%, suivi du gazole 15% et du charbon 7% ; 40% des PCB proviennent du bois, 30% du charbon et 14% des fiouls ; la moitié du HCB vient de la combustion des déchets, le bois et le gazole y contribuent chacun pour environ la moitié du reste.
2-2-2-3 Impact sanitaire de la pollution atmosphérique
Les filières carbonées de l’énergie participent à la pollution atmosphérique dans son ensemble mais il n’est pas possible d’identifier directement leur part respective dans l’impact sanitaire de cette pollution. C’est l’ensemble du cocktail formé par les différentes sources qui constitue l’agent toxique.
On peut par contre établir des relations entre différents marqueurs co-variants de la pollution et différents indicateurs de santé. Les relations les plus robustes sont établies à partir des marqueurs : particules (PM10 et PM2 ,5), NOx et ozone.
La part respective des différentes filières à l’impact sanitaire de la pollution atmosphérique peut être approchée indirectement à partir de ces corrélations. La nature exacte du ou des toxiques impliqués, ou de leur interaction, demeurant cependant mal connue la fiabilité de cette démarche reste faible.
Deux types d’études épidémiologiques permettent d’étudier 1 -les effets à court terme des pics de pollution et 2 - les effets à long terme de la pollution de fond. Les effets à long terme de la pollution sont de très loin les plus préoccupants, ils se manifestent à tous les niveaux actuels de la pollution urbaine et rurale par des milliers de cas de maladies cardiovasculaires, bronchopulmonaires et de cancers du poumon.
En termes de mortalité à court terme l’impact incrémentiel de 10 µg de PM2,5 est de l’ordre de 0,6% ; en termes de mortalité correspondant à une exposition sur le long terme il est de l’ordre de 5%. Les maladies cardiopulmonaires y contribuent majoritairement.
Il existe cependant une assez large variabilité des résultats laissant place à une large incertitude.
Certaines maladies systémiques semblent également induites par les niveaux de pollution actuels sans que l’on puisse préciser le niveau de risque.
Il n’est pas possible d’évaluer directement l’impact sanitaire de chacun des constituants toxiques émis dans l’atmosphère par les sources carbonées de l’énergie. Par contre on connaît assez bien ce qui résulte de l’inhalation de l’ensemble des particulles atmosphériques auxquelles contribuent ces émissions de manière très significative, associées aux particules provenant de l’érosion naturelle et de celles provenant de diverses opérations de broyage industriel des roches dont on sait qu’elles ont une toxicité relativement faible [27].
Différents indicateurs caractérisent la pollution atmosphérique, on retient plus particulièrement les teneurs en SO2, NOx, ozone et COVNM pour la partie gazeuse et PM10, PM2,5 correspondant aux particules de moins de 10 micromètres et de moins de 2,5 micromètres de diamètre respectivement pour la pollution particulaire.
Mettre en corrélation la variation de concentration de ces indicateurs avec différents indicateurs de santé permet d’établir des relations dose-effet. Ces indicateurs de santé concernent en particulier : - la mortalité toutes causes et la mortalité spécifique d’origine pulmonaire, cardiovasculaire et la mortalité par cancer ; - et la morbidité basée sur le nombre d’hospitalisations, la prise de consultations et de divers médicaments comme ceux destinés à traiter les crises d’asthme.
Schématiquement deux types d’études sont déployées : 1 - celles qui établissent les corrélations temporelles journalières entre les variations de concentration des indicateurs de pollution et les varaitions simultanées des indicateurs de santé ; 2 - celles qui analysent dans la durée les conséquences lointaines de l’exposition aux polluants atmosphériques.
Les études du premier type permettent d’identifier les effets immédiats et peu retardés de la pollution atmosphérique et sont relativement simples à mettre en œuvre à partir du moment où on peut assurer un maillage satisfaisant de la dosimétrie des polluants et disposer de statistiques médicales fiables. Dans les études de mortalité précoce les corrélations temporelles permettent de constater une augmentation de la morbidité et de la mortalité imputable à l’exposition mais elles ne renseignent pas sur la perte moyenne d’années de vie qui leur est associée.
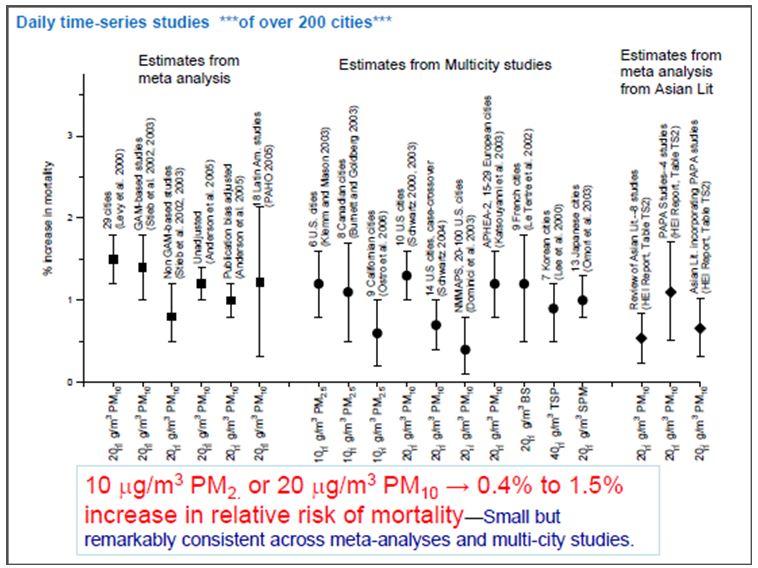
De nombreuses études ont permis d’évaluer l’impact des particules, CA Pope en a proposé une synthèse pour l’EPA en 2011[28] dont les résultats apparaissent dans la figure 3. Une augmentation des particules atmosphériques de 10 à 20 microgrammes par m3 d’air est corrélée avec une augmentation de 0,4 à 1,5% de la mortalité due à la pollution atmosphérique.
Figure 3 Mortalité associée aux variations de 10 à 20 microgrammes de particules atmosphériques dans différentes parties du monde ; évaluation à partir des corrélations temporelles ne dépassant pas une semaine.
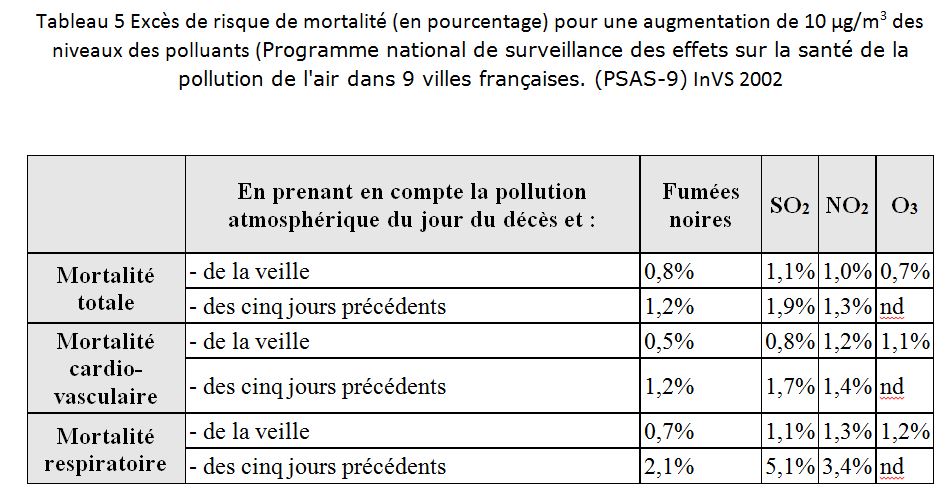
D’autres indicateurs de la pollution de l’atmosphère donnent des résultats globalement cohérents témoignant essentiellement du caractère traceur des ces indicateurs et non de leur toxicité (les effets ne s’additionnent pas) comme par exemple Tableau 5.
Bien que les différences observées suggèrent la possibilité d’une relation causale les indicateurs sont trop interdépendants et les intercomparaisons trop inconstantes pour attribuer à chaque polluant la part des décès observés.
Pour étudier les effets tardifs des expositions chroniques, études de type 2, il est nécessaire de suivre pendant un temps prolongé des cohortes constituées de sous-groupes stables exposés durablement à des niveaux différents d’exposition. Les caractéristiques doivent être reconstituées avec le maximum de fiabilité pendant toute la durée de l’étude pour pouvoir être mises en corrélation avec les indicateurs de santé. Ces cohortes permettent notamment d’évaluer par tranche d’âge la perte moyenne d’années de vie perdues en fonction des expositions accumulées mais elles ne permettent pas d’identifier qui en a été particulièrement victime.
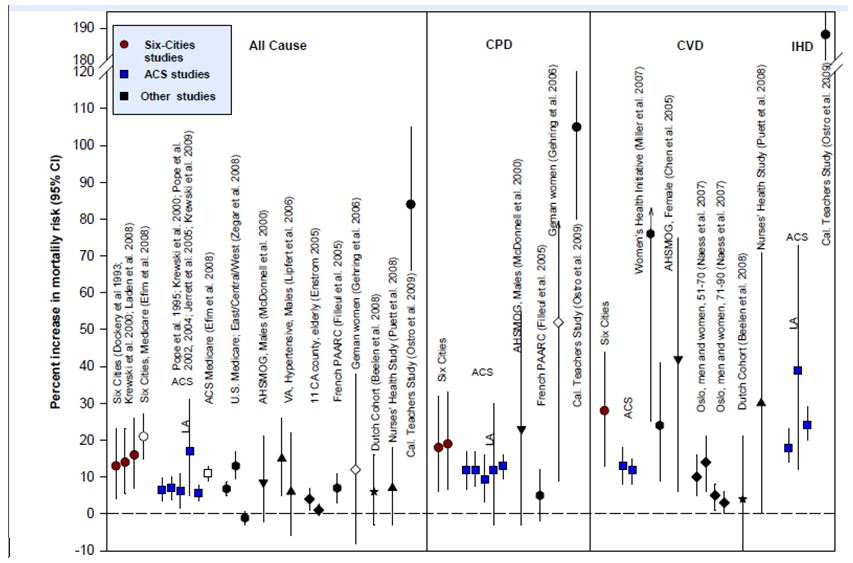
CA Pope a proposé en 2011[29] une synthèse conclusions des principales études disponibles concernant ces cohortes exprimant les excès de mortalité : toutes causes, cardiopulmonaire (CPD), cardiovasculaire (CVD) et cardiopathies ischémiques (IHD). Les résultats apparaissent dans la figure 4.
Figure 4. Excès de mortalité associés dans différentes cohortes à une augmentation de 10 µg/m3 de particules fines dans l’atmosphère.
Légende
All causes : mortalité toute cause ; CPD : mortalité cardiopulmonaire ; CVD : mortalité cardivasculaire ; IHD : mortalité par ischémie cardiaque
La validité de ces corrélations est confirmée avec le développement des politiques de réduction des expositions. Il a été ainsi possible de constater la diminution du taux de mortalité corrélée avec la diminution d’exposition aux particules fines en utilisant les mêmes indicateurs et la même méthodologie[30]
Les résultats sont caractérisés par une grande variabilité qui peut refléter à la fois la diversité des cohortes et celle des constituants toxiques. Pour la mortalité toutes causes, indicateur essentiel de l’impact sanitaire, une métaanalyse a été proposée en 2013 par Hoek et al[31], mise à jour par l’OMS après les résultats de la cohorte européenne Escape (367 250 participants suivis pendant 14 ans). Elle aboutit à la valeur de risque relatif de 1,07. La valeur propre à Escape est de 1,14 mais elle a une puissance statistique faible devant les millions de participants aux enquêtes américaines et n’influence que peu les résultats de la méta analyse. Cette valeur centrale attribuant un excès de mortalité de 7% par incrément de 10 microgammes par m3 de PM2,5 comprend néanmoins une large incertitude.
L’importance de l’incertitude a été évaluée au Royaume Uni par l’étude COMEAP 2010[32] qui conclut que l’excès de mortalité par 10 microgrammes par m3 de PM2,5 est compris entre 1 et 12% avec une probabilité évaluée à 0,75. En termes de mortalité attribuable cela correspondrait à une évaluation comprise entre 4 700 et 51 000 décès en 2008 pour l’ensemble des populations anglaises et galloises.
Ainsi la très grande majorité des décès attribuables, malgré les incertitudes, est bien due aux effets tardifs de la pollution de fond et non aux pics de pollution. Elle se manifeste aux niveaux actuels observés en France soit en moyenne entre 10 et 15 mg/m3 pour les PM2,5[33].
La part relative aux pathologies spécifiquement associées à la pollution atmosphérique fait l’objet d’évaluations variables pour ce qui concerne les 3 principales : pulmonaires, cardiaques et vasculaires et cancer du poumon. Sur la base des enquêtes américaines les maladies cardiaques et vasculaires, constamment retrouvées dans toutes les enquêtes, sont à l’origine de la grande majorité des décès prématurés, suivis par les maladies pulmonaires et le cancer. Pour le cancer une valeur centrale dégagée par la méta analyse[34] se situe à environ 9% des nouveaux cas de cancer du poumon par 10 µg de PM2,5 ou PM10, mais cette valeur peut atteindre jsqu’à 22 % dans l’étude Escape concernant les populations urbaines d’Europe[35]. Ces différences d’évaluation peuvent être dues au tabagisme. Dans la méta analyse l’effet cancérogène des particules est minimal chez les fumeurs (6%) et maximal chez les anciens fumeurs (44%).
Les études concernant la morbidité sont moins nombreuses que celles concernant la mortalité, notamment pour ce qui concerne les effets chroniques ; de nombreuses lacunes entachent l’évaluation de l’impact global. Les corrélations les mieux établies concernent le lien avec l’asthme chez l’enfant et les pathologies broncho pulmonaires chez les patients de plus de 65 ans[36]. Pour les pathologies cardiaques et vasculaires le lien est plus inconstant. Des données récentes établissent cependant un lien entre athérosclérose et pollution atmosphérique, confirmé par la mise en evidence d’indicateurs spécifiques de la souffrance vasculaire induite par les PM 2,5[37]
Des liens plus ténus ont été suggérés entre pollution atmosphérique et diverses maladies dont le diabète de type 2, les maladies rénales, l’infertilité, la prématurité à l’accouchement, le développement neurocognitif, l’autisme, la maladie de Parkinson, et divers cancers, toutes conséquences qui ne peuvent actuellement être quantifiées. Pour les maladies létales cependant le bilan de l’ensemble ne peut conduire à une évaluation supérieure à celle dont on dispose par les études de mortalité toutes causes, évaluation déjà largement couverte par la somme des décès attribuables aux maladies cardiopulmonaires et cardiovasculaires fortement liées à la pollution.
2-2-2-4 Effets toxiques identifiés
Certains composants de la pollution atmosphérique : CO, dans des conditions accidentelles, SO2 associé aux grands smogs historiques et l’ozone signent indiscutablement leurs effets au-delà de concentrations seuils qui peuvent être rencontrées dans l’air ambiant.
Les concentrations atteintes par les oxydes d’azote se situent en deçà de valeurs associées à des effets toxiques
L’inhalation de particules atmosphériques de l’aérosol urbain est associée à de multiples effets qui dépendent du territoire de dépôt particulaire dans les voies aériennes. La fraction PM10 est associée avec une irritation bronchique ; la fraction PM2,5 est associée à une souffrance des cellules vasculaires ; la composante ultrafine échappe à la séquestration locale et migre par voie sanguine vers divers organes. Le mécanisme toxique le plus constant est l‘induction d’un stress oxydant.
Il n’est pas possible de distinguer si l’effet toxique vasculaire des PM2,5 est de nature physique ou associé à des toxiques minéraux et organiques adsorbés. Il y a consensus pour estimer que les particules naturelles provenant des embruns et de l’érosion ne sont pas iimpliquées alors que les particules riches en carbone le sont systématiquement. Il y a débat sur le rôle attribué aux particules de sulfates et de nitrates.
En pratique l’ozone, pour les effets aigus, et les particules pour les effets aigus et chroniques, sont les indicateurs d’exposition les plus pertinents pour caractériser les relations dose-effet. Les effets se manifestent au lieu d’émission et à des distances qui peuvent atteindre plusieurs centaines de Km.
Dans la gamme des concentrations environnementales observées, une relation dose effet linéaire sans seuil rend compte de la majorité des observations épidémiologiques. Cette relation ne repose pas sur un mécanisme toxique plausible permettant d’extrapoler l’observation.
L’évaluation d’effets systémiques éventuellement dus à l’impact des neurotoxiques, cancérogènes et mutagènes émis dans l’environnement lors de la combustion des sources carbonées doit être évaluée indirectement à partir de modélisations.
Monoxyde de carbone CO. L’oxyde de carbone poison de l’hémoglobine dont il déplace l’oxygène transporté vers les tissus, est à l’origine de plus de 3000 intoxications déclarées en France chaque année et d’une centaine de décès provoqués à domicile par des installations de chauffage défectueuses. L’exposition chronique est associée avec un risque de cardiopathie ischémique.
Aux concentrations habituelles de l’air ambiant les niveaux de CO sont 50 fois inférieurs au seuil de toxicité[38]
Historiquement S02 est associé aux épisodes dramatiques de pollution comme le grand smog de Londres de 1952. Les émissions actuelles ne conduisent pas à de telles concentrations atmosphériques supérieures à 500 µg/m3, seuil d’effets toxiques pour une exposition courte. Il existe cependant des corrélations mettant en évidence un excès de mortalité toutes causes de l’ordre de 0,5% par dépassement de 10 µg/m3 pour 24 h d’exposition aux niveaux contemporains d’exposition de l’ordre de la dizaine de µg/m3. Il est également mis en évidence des corrélations fortes avec les admissions hospitalières pulmonaires et cardiovasculaires, en particulier chez les enfants asthmatiques[39]. Ces corrélations interviennent dans le contexte du mélange de polluants que représente l’aérosol urbain. Le rôle des sulfates particulaires peut contribuer à ces résultats. Dans l’étude de cohorte de villes américaines la diminution de mortalité associée à la diminution d’exposition aux PM2,5 de 2002 à 2007 est corrélée de manière sélective à la diminution des sulfates[40].
Le rôle des oxydes d’azote est disputé. NO n’est pas toxique, c’est un médiateur de nombreuses réactions biologiques ; dans l’atmosphère il se transforme rapidement en dioxyde N02 toxique mais les niveaux atteints n’atteignent que très rarement le seuil de toxicité chez l’homme situé au-dessus de 0,2ppm (environ 400 µg/m3) lorsqu’il est inhalé seul. NO2 apparaît cependant comme un cofacteur important associé à la phase particulaire, impliqué dans les troubles du développement des fonctions pulmonaires de l’enfant, avec un déficit concernant 7% de la population par augmentation de 10 µg/m3 de NO2 dans les atmosphères urbaines[41]. NO2 est associé d’une manière constante à la mortalité toutes causes et à la mortalité cardiopulmonaire dans les études épidémiologiques, les résultats sont plus inconstants pour ce qui concerne les effets cardiovasculaires [42]. Pour les liens avec le cancer du poumon les résultats sont inconstants mais la méta analyse[43] conduit à une évaluation d’un excès de 4% par 10 µg/m3 de NO2 sans que l’on puisse y voir autre chose qu’une corrélation avec un marqueur ubiquitaire de la pollution urbaine. Les oxydes d’azote participent en outre à la formation d’ozone et à celle du toxique peroxy-acyl-nitrate par réaction photochimique. On admet cependant que l’essentiel de la toxicité des oxydes d’azote est dû à la nucléation de nitrates, constituants majeurs de la phase particulaire fine.
L’ozone et la phase particulaire constituent les 2 constituants toxiques les plus constamment impliqués dans les maladies imputables à la pollution atmosphérique.
Les effets sanitaires de l’ozone atmosphérique peuvent être distingués de ceux de la pollution particulaire dont les pics de pollution sont fréquemment séparés, cependant une covariable thermique constante y est associée et complique les évaluations. En outre ozone et NOx sont étroitement liés.
Les effets toxiques de l’ozone seul sont détectables chez l’homme à partir de 120 µg/m3, notamment par la mise en évidence de marqueurs biologiques, comme les produits d’oxydation des lipides du film alvéolaire et le dosage du NO endogène dans l’air expiré. Ces deux marqueurs traduisent une réaction inflammatoire locale.
Sur la base des hospitalisations en relation avec les pics d’ozone, un seuil d’effet toxique a été proposé entre 80 et 100 µg/m3 cependant cette conclusion est contestée. La forme de la relation dose effet est complexe, avec une inflexion traduisant un effet d’adaptation aux fortes concentrations.
La synthèse la plus récente du document Revihaap de l’OMS[44] concernant les effets à court terme de l’ozone résultent de la combinaison des données européennes et américaine APHENA. Les résultats impliquent qu’à une augmentation de 10 µg/m3 de la concentration ambiante sont associés des excès : de mortalité toutes causes de 0,18% ; de mortalité cardiovasculaire chez les personnes de plus de 75 ans de 0,22% ; de mortalité cardiovasculaire chez les plus jeunes de 0,35% ; de mortalité pumonaire de 0,19%, avec une augmentation équivalente des hospitalisations chez les plus de 65 ans.
Les effets à long terme de l’exposition à l’ozone font l’objet de débats. A l’heure actuelle la meta analyse des données ne permet pas de conclure à un effet spécifique de l’exposition à long terme à l’ozone[45].
La phase particulaire, avec une expression variable selon le niveau de coupure granulométrique : PM10 pour les particules de taille inférieure à 10 µm, PM2,5 et PM1 moins de 2,5 µm et 1 µm respectivement, et encore ultrafines nanométriques ou divers substituts comme ‘’fumées noires’’, ne constitue pas une classe définie de toxiques, dans la mesure où la composition chimique et les propriétés physiques de ses constituants sont largement variables. Il n’en demeure pas moins que ces particules peuvent être, avec certitude, reliées à un effet toxique commun directement mis en évidence par des corrélations avec les variations journalières des marqueurs de l’inflammation. Il en est de même pour les corrélations avec le stress oxydant et les altérations de l’électrocardiogramme[46]. Dans l’étude récente de Pope et al 2016[47] les pics de pollution aux PM 2,5 étudiés pendant 3 années sur de jeunes volontaires sains non-fumeurs sont corrélés avec des marqueurs de souffrance des cellules vasculaires, avec la diminution des facteurs de revascularisation, avec une augmentation des monocytes et des T lymphocytes circulants, tous facteurs impliqués dans les pathologies tardives cardiovasculaires.
Lorsque les études permettent de distinguer les PM10 des PM2,5 il est noté que les PM10 ont un impact fort sur les effets à court terme concernant les pathologies pulmonaires des voies hautes mais pas des bronchioles. Ceci s’explique par un dépôt faible dans les voies basses. Par contre si les effets cardiovasculaires des 2 types de particules sont comparables dans les études à court terme, l’impact à long terme des PM10 sur la mortalité cardiovasculaire n’est pas établi, contrairement à celui des PM2,5 dont le dépôt atteint le lit très vascularisé.
Parmi les constituants variables des PM la présence de carbone élémentaire ou organique a fait l’objet d’attentions particulières. Les conclusions de l’OMS (Revihaap[48]) sont que les particules de carbone ne sont pas en elle-même des toxiques mais qu’elles sont le support privilégié d’adsorption des différents toxiques agissant sur et à distance du poumon. Cette propriété est partagée par les sulfates particulaires. A noter cependant que les particules ultrafines de carbone ont une action directe démontrée sur le rythme cardiaque et sur l’électrocardiogramme.
L’aérosol urbain comprend un contingent de particules ultrafines, nanométriques, dont la composition en divers toxiques organiques et inorganiques est enrichie par rapport à la masse globale de l’aérosol. Les propriétés particulières des nanoparticules leur permettent d’échapper à la séquestration par les macrophages et de diffuser dans le sang et différents organes dont le cœur, le rein et le cerveau. Ces propriétés font suspecter les particules ultrafines d’avoir un impact important dans les pathologies de la pollution atmosphérique mais on ne dispose pas d’études épidémiologiques permettant de l’évaluer.
Une part très importante de la phase particulaire est faite de nitrates et de sulfates formés à partir de NO2 et de SO2. Les études cliniques et toxicologiques ne permettent pas de leur attribuer un potentiel toxique aux niveaux où ils se trouvent dans l’environnement. Cependant, en tant que constituants de l’aérosol urbain ils ont été associés à différentes pathologies pulmonaires et cardiovasculaires. Les résultats sont cependant inconstants, plus robustes pour les sulfates que pour les nitrates. L’une des hypothèses retenues pour expliquer leur rôle en tant que toxiques est leur combinaison avec des toxiques métalliques et organiques comme les HAP (Revihaap).
Bien qu’ils soient impliqués dans la génération de radicaux oxydants les études toxicologiques n’ont pas permis d’identifier de métaux spécifiquement associés aux pathologies induites par la pollution atmosphérique[49] . Cependant une corrélation a été mise en évidence entre la concentration en nickel et diverses altérations temporaires de la fonction cardiaque et le groupe cuivre-zinc-vanadium a été associé avec une augmentation temporaire du fibrinogène sanguin. Dans les études épidémiologiques concernant le cancer et les éléments Cu, Fe, K, Ni, S, Si, V et Zn dans les PM10 et PM2,5 des corrélations existent avec tous éléments à l’exception du vanadium ; le soufre et le nickel donnent les corrélations les plus fortes[50].
Différentes études caractérisent l’impact sanitaire de la phase particulaire en fonction de la source carbonée d’origine. Dans l’étude des 6 cités US, les sources dérivées du pétrole comme celles dérivées du charbon sont liées à la mortalité alors que les particules provenant de l’érosion ne le sont pas [51]. Dans l’étude récente de 100 zones urbaines aux USA la part des particules provenant de la combustion du charbon dans les PM2,5 se révèle 5 fois plus néfaste pour la mortalité par cardiopathie ischémique que la moyenne des PM2,5[52]. Cette étude ne trouve pas de relation avec les PM2,5 provenant de l’érosion des sols ni de la combustion de la biomasse. Globalement il y a débat sur la combustion de la biomasse, fortement associée aux effets néfastes de la pollution domestique (Revihaap) mais marquée par les résultats inconstants entre la mortalité journalière et le niveau épisodiquement élevé de PM2,5 provenant des grands feux de forêts[53].
Les mécanismes toxiques mis en évidence après inhalation des particules de l’aérosol urbain mettent en jeu le stress oxydant et des réactions diverses du système nerveux autonome. Il en résulte une cascade de médiateurs de l’inflammation avec une cible particulière constituée par les cellules vasculaires. Les effets à distance de la voie pulmonaire d’entrée s’expliquent par la solubilisation de composés toxiques et par la migration particulaire dans le cas des particules ultrafines.
A l’exception des agents génotoxiques, qui sont susceptibles d’altérer l’ADN de manière aléatoire aux doses les plus faibles et participer à la cancérisation des tissus, aucun mécanisme toxicologique ne permet de d’envisager l’absence de seuil pour les effets sur la morbidité et la mortalité pulmonaire et cardiovasculaire, même en tenant compte de l’existence de groupes fragiles. Néanmoins, dans la gamme d’exposition aux particules environnementales, entre 5 et quelques dizaines de µg de PM2,5/m3 tout se passe comme si, avec les larges marges d’incertitude caractérisant les mesures effectuées, la relation exposition effet pouvait être considérée comme linéaire et sans seuil.
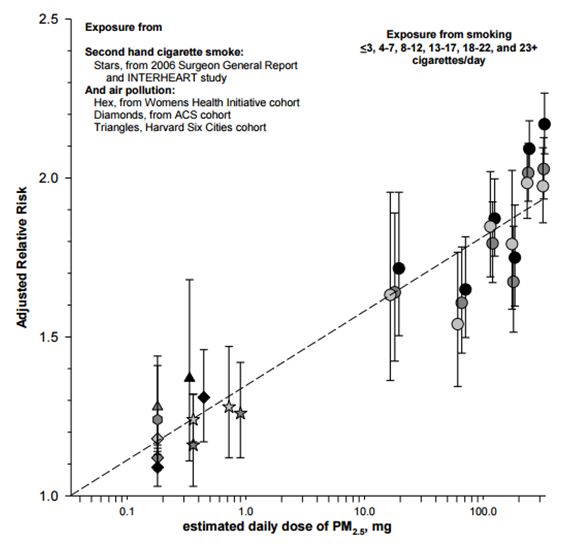
En fait quand on intègre les données correspondant aux fortes expositions la linéarité ne tient pas et des relations plus complexes, avec une forte atténuation aux expositions fortes, doivent être envisagées[54]. Il est donc vraisemblable que la forme de la relation dose effet soit en fait une montée rapide, au-delà d’un seuil inférieur à 5 µg/m3[55] suivie d’une croissance pratiquement linéaire, prolongée d’une inflexion aux fortes expositions qui tire la relation exposition effet vers une relation semi logarithmique. C’est ce qui apparaît das la figure 5 où le risque relatif de développer des maladies pulmonaires et cardiovasculaires est exprimé en fonction d’une échelle logarithmique exprimant la quantité totale pumonaire inhalée, provenant des aérosols urbains, de l’enfumage passif et du tabagisme. Cette figure illustre en outre la similitude de réponse à des aérosols de nature très différente et constitue un argument pour considérer la phase particulaire comme un toxique générique.
Fig 5 Pope et al 2011[56]. Forme de la relation exposition entre le coefficient de risque relatif et le logarithme de la quantité totale inhalée journalière provenant d’aérosols urbains, du tabagisme passif à gauche et du tabagisme actif à droite, pour différentes maladies pulmonaires et cardiovasculaires.
2-2-2-5 Hypothèses faites pour l’évaluation des conséquences sanitaires des différentes sources d’énergie carbonée.
C’est à partir des relations exposition effet qui caractérisent mortalité et morbidité associées à la pollution atmosphérique qu’on évalue l’impact spécifique des différentes énergies carbonées. L’hypothèse de base est que les toxiques impliqués sont communs aux différentes sources et peuvent être modélisés à partir de quelques constituants. Ce travail a été particulièrement développé par le groupe de travail européen ExternE (External costs of Energy) de 1995 à 2005 et dans une mesure moindre et avec la même methodologie aux Etats Unis [57] .
Aux particules exprimées en PM10, pour les effets aigus, et aux PM2,5, pour les effets chroniques, est associé l’essentiel de l’impact sanitaire. On ajoute les effets aigus de l’ozone qui peuvent être distingués de ceux des particules et on prend en compte les effets systémiques des métaux et composés organiques toxiques bien que cela ne modifie que peu l’impact global [58].
Dans cette perspective SO2 et NOx sont uniquement pris en compte pour leur impact sanitaire en tant que sources de particules. Bien qu’il n’existe pas de données toxicologiques permettant d’évaluer leur potentiel, la revue de la littérature disponible a incité ExternE à décider que : les nitrates avaient 0,5 fois la toxicité des PM10 et que les sulfates avaient la toxicité des PM10, particules elles-mêmes affectées de 0,6 fois la toxicité des PM2,5. Il a été également convenu que les particules primaires émises à la cheminée par les centrales de production étaient équivalentes aux PM10 alors que celles provenant des sources mobiles de la circulation routière avaient 1,5 fois la toxicité des PM2,5.
L’évaluation de l’impact sanitaire nécessite en outre de modéliser la dispersion des polluants depuis leur source d’émission jusqu’à plusieurs milliers de km, en tenant compte des caractéristiques propres à chaque installation. Ces polluants sont transportés par le vent et dilués par turbulence jusqu’à ce qu’ils soient déposés par voie sèche ou par la pluie.
Les aérosols primaires sont peu modifiés à moins de 50 km de l’émission, leur modélisation dans ExternE est assurée par un modèle simple gaussien de propagation en ligne droite. Par contre à distance plus lointaine des réactions chimiques interviennent dans l’atmosphère et aboutissent à la formation des polluants secondaires, ozone, sulfates et nitrates, la modélisation de leurs comportements est effectuée avec des modèles lagrangiens plus complexes. Les caractéristiques des émissions, massives, localisées et fixes à la cheminée des centrales nécessitent en outre une modélisation différente de celle des sources mobiles.
Ces modélisations ont pu faire l’objet de validations à partir de mesures réelles dans certaines circonstances. Des variations d’un facteur de l’ordre de 2 ont été observées [59].
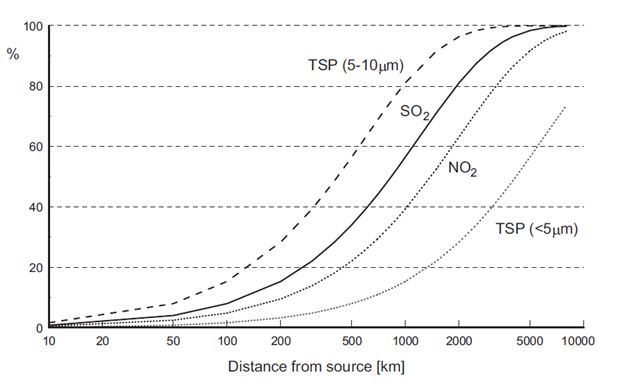
La synthèse à partir de ces modèles donne une évaluation des dommages attendus en fonction de la distance à la source fig 6
Fig 6 Modélisation de la répartition des dommages cumulés attendus en fonction de la distance à la source dans ExternE Methodology update 2005.
Noter l’importance de la dissémination des particules en suspension (TSP) de taille inférieure à 5µm dont 50% de l’impact se titue au-delà de 5.000Km
Pour les polluants systémiques la modélisation doit être plus complète pour tenir compte du dépôt au sol et du transfert dans l’eau et les différents échelons de la chaîne alimentaire. L’ingestion peut ainsi constituer pour certains toxiques la voie prépondérante d’impact (As, Hg, Pb, dioxines). Par contre l’action cancérigène du formaldéhyde, du CrVI, du Ni et du Cd n’est observée qu’après inhalation et ne justifie pas de prendre en compte la pollution de la chaîne alimentaire[60].
2-2-2-6 Bilan sanitaire des énergies carbonées.
La quantification de l’impact sanitaire demande à choisir les paramètres pertinents des relations exposition effet ou concentration effet. Pour les particules et l’ozone ces paramètres sont issus de l’épidémiologie de la pollution atmosphérique. Ils dérivent de l’hypothèse de linéarité sans seuil[61] appliquées aux relations entre la concentration dans l’air d’une part et morbidité et mortalité d’autre part.
Parmi les valeurs possibles ExternE 2005 retient
Pour les effets aigus des premiers jours:
Une augmentation de 0,6% de la mortalité par augmentation de 10µg/m3 de PM10
Une augmentation de 0,3% de la mortalité pour une augmentation moyennée sur 8h de 10µg d’O3
Pour la mortalité infantile dans la première année,
après une exposition dans les 2 premiers mois de la vie : Une augmentation de 4% par 10µg de PM10
Pour les effets chroniques :
Une augmentation de 5% de la mortalité par augmentation de 10µg de PM2,5. Cette évaluation inclut la mortalité induite par les effets aigus.
En termes de morbidité plusieurs indicateurs de santé sont disponibles pour les PM10 par 10 µg/m3 et par an :
- Nouveaux cas de bronchite chronique : pour 100.000 adultes : 26,5 cas
- Hospitalisations - pour maladies respiratoires : pour 100.000 personnes de la population générale 7,03 cas ; - 4,34 cas pour les hospitalisations en cardiologie.
- Nombre de consultations pour asthme : pour 1000 patients : 1,18 pour la tranche d’âge de 0-14 ans ; 0,5 pour la tranche d’âge 15-64 ans ; et 0,95 pour les plus de 65 ans.
- Nombre de-consultations en otho-rhinolaryngologie pour 1000 patients : 4 pour la tranche d’âge 0-14 ans ; 3,2 de 15à 64 ans et 4,7 pour les plus âgés.
- Jours d’utilisation de bronchodilatateurs chez 1000 asthmatiques : 180 chez les enfants de 5-14 ans et 912 chez les adultes avec un asthme confirmé
- Aggravation des symptomes chez les patients atteints de maladies respiratoires chroniques : augmentation de 30%
Et pour les effets imputables à l’ozone, exposition moyennée sur 8h, par année et par 10 µg/m3
- Hospitalisations par 100.000 personnes de plus de 65 ans : 11,5
- Consultations pour rhinite allergique pour 1000 patients : 3 pour les enfants de 0 à 14 ans et 1,6 pour les personnes âgées de 15 à 64 ans
- Jours d’utilisation de bronchodilatateurs chez 1000 asthmatiques : 310 pour les enfants de 5 – 14 ans ; 730 pour les asthmatiques confirmés de plus de 20 ans
En dehors de ces effets directement mis en évidence par l’épidémiologie, d’autres peuvent être prévus à partir de modélisation. ExternE recommande de retenir les paramètres de l’EPA-IRIS pour l’évaluation des cancérogènes systémiques.
Dans le cas du plomb où le risque avéré est une diminution du QI proportionnelle à la quantité absorbée pendant les 2 premières années, le paramètre retenu est de 0,014 points de QI par année par µg/m3 par personne de la population générale. Cette évaluation tient compte de la fraction de population âgée de moins de 2 ans et du coefficient de corrélation liant la concentration de plomb dans l’air à celle de la plombémie incluant la part imputable à l’ingestion après dépôt au sol.
2-2-2-7 Evaluation de la perte d’espérance de vie
Dans la majorité des cas les indicateurs de dommages sanitaires sont exprimés en risque relatif traduisant le ratio du nombre de cas observés après exposition à un excès de concentration du toxique concerné par rapport au nombre de cas existants sans cet excès d’exposition.
La relation entre mortalité et concentration en PM2,5 en Europe peut être décrite[62] par une fonction log linéaire simple : Dy = y0 (1 – e-ß∆x) où DY est la baisse du nombre de décès qui serait associée à une baisse DX de la concentration des PM2,5 ; b est la pente de la relation entre le logarithme de la mortalité et la concentration en PM2,5 ; dans le cas d’un risque relatif RR, observé pour une exposition à un 10µg/m3 la valeur est : b = ln(RR/10).
La probabilité de diminution de décès par tranche d’âge est elle-même dépendante du même facteur e-ß∆x. L’utilisation des tables de mortalité donnant la probabilité de survie aux différents âges de la vie permet de calculer les gains attendus par l’exposition évitée, en général exprimée pour un gain de l’espérance de vie à 30 ans. Les impacts sur la population infantile demandent une autre approche.
ExternE utilise une méthode un peu différente avec des résultats très comparables à ceux dérivés de l’utilisation des tables de mortalité. Il en résulte une expression simplifiée[63] reliant de manière proportionnelle la concentration en PM2,5 à la perte d’années de vie, dans la gamme des expositions usuelles. Cette propriété, malgré les déterminants non linéaires qui la conditionnent, permet de définir pour l’Europe une valeur générique de 0,22 jour de vie perdue par exposition de 1 an à un excès de 1µg/m3.
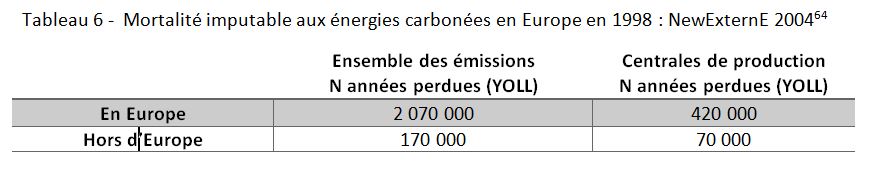
Une synthèse a été proposée pour l’ensemble de l’Europe soumise aux retombées de production des énergies carbonées, prenant en compte la densité des populations affectées par la dispersion locale du panache ajoutées aux données dérivées du modèle régional, Tableau 6.
Pour un total de 2,2 millions d’années perdues, avec une perte par cas évaluée à 5 ans, ces chiffres correspondent à environ 450 000 décès prématurés pour l’année 1998.
2-2-2-8 Ventilation des dommages en fonction de la distance
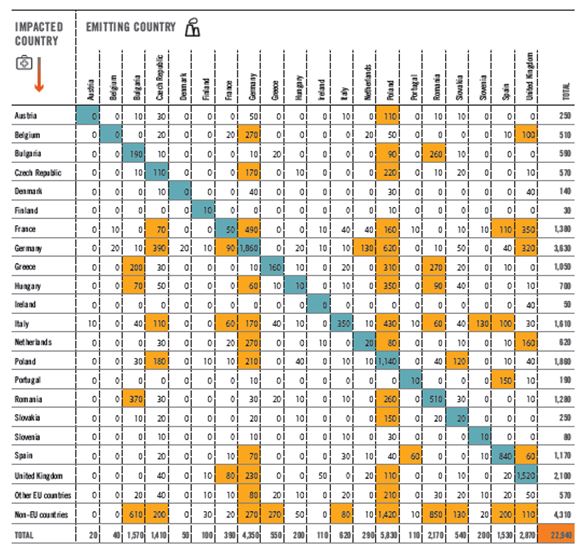
Il est possible de faire un bilan de l’impact au-delà des frontières des émissions à partir de leurs sources fixes, comme cela a été fait pour les centrales à charbon en Europe à partir des mesures à la source et de la modélisation locale et régionale de la dispersion tableau. 7
Tableau 7-Décès prématurés imputables en 2013 aux différentes centrales thermiques à charbon européennes. Chaque ligne permet de connaître la contribution des différents pays aux décès prématurés dans chacun d’entre eux. Les cases orangées signalent des excès supérieurs à 50, les cases bleues la part nationale de la contribution totale : Europe’s Dark Cloud 2016[65]
2-2-3 Autres sources d’énergie
L’essentiel des effets sanitaires associés aux autres types d’énergie, en dehors des situations accidentelles, résulte de l’impact dû à l’usage des énergies carbonées au cours de leur cycle de vie.
La particularité essentielle propre aux filières éolienne et photovoltaïque tient au fardeau sanitaire que présentent les métaux lourds nécéssaires à leur mise en œuvre.
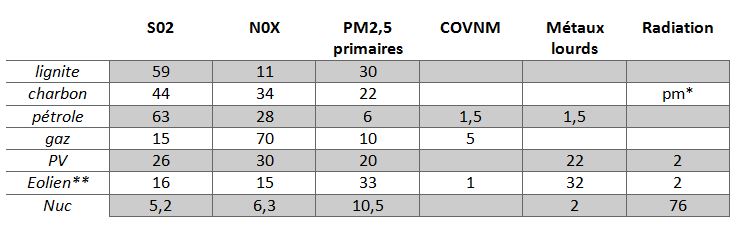
Par comparaision l’importance des différents acteurs du dommage sanitaire pour les différentes filières, notamment non carbonées, a été évaluée dans NewExternE 2004. Elle apparaît dans le tableau 8 qui ne renseigne pas sur les méfaits relatifs des différentes filières mais indique pour chacune l’’importance relative de la contribution des toxiques qui y sont associés.
Tableau 8 Part respective de 100% des dommages sanitaires attribués aux polluants primaires pour différentes sources d’énergie d’après NewExternE 2004
** Un point particulier concerne les inconvénients provoqués par les éoliennes où des effets sont imputés essentiellement au bruit, en particulier aux infrasons. Les symptômes allégués concernent : troubles du sommeil, maux de tête, vertiges, acouphènes. Une récente métaananalyse ne confirme cependant pas le lien causal avec l’exposition au bruit, tout au plus fait-elle apparaître un seuil d’acceptabilité pour un fond sonore inférieur à 35dB[66] . Les mesures effectuées sur le terrain montrent par ailleurs que la protection offerte par la limitation des fréquences audibles garantit la protection contre les infrasons[67]. Ces points sont confirmés par l’ANSES[68] qui ne retient pas l’hypothèse d’une maladie vibro acoustique spécifique mais identifie un syndrome éolien d’intolérance environnementale à l’origine des nombreuses plaintes de riverains. Quelle qu’en soit la cause, qui reste débatue, le bilan épidémiologique de cette nuisance reste à faire.
2-2-4 Normalisation et comparaison des risques en matière de production d’électricité
Les résultats des synthèses européennes et américaines sur les externalités de l’énergie ont permis de hiérarchiser les filières en fonction des dommages attribués par TWh. Le résultat peut être exprimé en pertes d’années de vie comme dans Rabl et Spandero[69] tableau 9 :
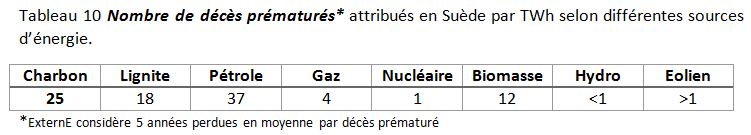
Le même travail par TWh effectué en Suède par Startfeld et Wickdahl[70] est exprimés en nombre de décès prématurés et correspond aux caractéristiques des émissions suédoises : tableau 10
*ExternE considère 5 années perdues en moyenne par décès prématuré
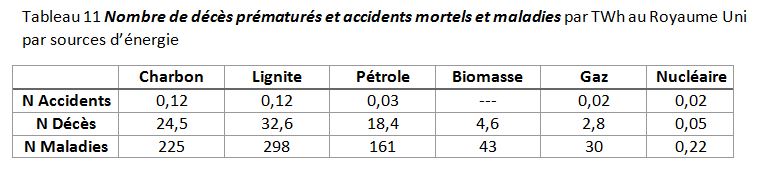
Et de manière plus complète par Markandya et Wilkinson[71] pour le Royaume Uni avec nombre de décès et accidents et nombre de cas de maladies sérieuses tableau 11
En termes d’effets sanitaires les choix des mix énergétiques influencent fortement les impacts globaux. En retenant les coefficents de risque par TWh de Rabl et de Markandya la comparaison des impacts attendus de la production électrique en 2015 laisserait prévoir : en France (546 TWh) 7300 années de vie perdues et 460 décès prématurés et en Allemagne (647 TWh) 41.300 années de vie perdues et 8400 décès prématurés
3 – Conclusion
De nombreuses inconnues demeurent quant à la quantification des dommages sanitaires imputables aux différentes énergies.
Pour ce qui concerne l’énergie nucléaire c’est surtout la validité des extrapolations de risque aux doses très inférieures à celles de la radioactivité naturelle qui peut être à l’origine de réévaluations. Toutefois la bonne connaissance des expositions et une longue expérience de validation des relations dose effet permettent une appréciation globale du risque peu susceptible d’être remise en cause pour les besoins de hiérarchisation des risques.
La gestion des accidents nucléaires pose cependant un problème non résolu : il s’agit de l’évaluation des dommages sanitaires indirects associés à long terme à la désorganisation des systèmes de soin et aux impacts des carences et des effets psychopathologiques imputables au chaos social laissé par la catastrophe. L’absence de prise en compte de cette composante à Tchernobyl a laissé place, dans les médias et chez certains scientifiques dissidents, à une évaluation confuse des causes de la dégradation sanitaire dans les régions affectées par l’accident. Le bilan de ces effets indirects peut être extrêmement lourd, il dépasse de loin celui des effets sanitaires radioinduits. La leçon a été retenue à Fukushima et a suscité une prise en charge précoce des populations. Cette attitude et les moyens d’aide et de contrôle épidémiologique mis en place devraient permettre de mieux connaître le coût de cette composante du risque sanitaire propre aux installations nucléaires.
Pour ce qui concerne les énergies carbonées la difficulté d’appréciation essentielle vient de la méconnaissance des interactions entre polluants atmosphériques. Il ne fait aucun doute que la pollution atmosphérique urbaine soit associée à une augmentation de la morbidité et de la mortalité à l’origine d’un décès prématuré sur 9 et de 9 mois de perte d’espérance de vie en Europe[72]. La difficulté demeure cependant d’en identifier les causes primaires et d’associer respectivement à chaque source de particules et de gaz une toxicité qui ne se manifeste que dans le contexte de mélange variable avec des constituants naturels et anthropogéniques d’autre nature.
Cette incertitude est la source probable des évaluations quelquefois peu cohérentes en matière d’effets sanitaires. En particulier les preuves directes de l’implication des sulfates sont relativement fragiles et celles des nitrates sont inexistantes, situation délicate car sulfates et nitrates constituent jusqu’à 80% de l’impact attribué au titre de leur contribution aux PM10 et PM2,5. En fait on ne dispose pas d’un indicateur d’exposition, qui soit en même temps un indicateur d’effet et permettrait une prévention optimisée par suppression sélective du ou des toxiques les plus impliqués.
Néanmoins l’ensemble de ces incertitudes n’affecte pas la hiérarchie générale des coûts sanitaires caractérisant les différentes filières de production d’énergie tant le coût des énergies carbonées est disproportionné par rapport à celui des autres filières. Ce coût laisse prévoir de l’ordre de 100 millions de décès prématurés à l’échelle mondiale pour une période d’exposition correspondant à une vie entière. Ce coût est suffisamment lourd pour qu’il impacte de manière significative celui des énergies non carbonées en amont et en aval de leur production, notamment pendant l’intermittence des ENRi.
Quel que soit le mode d’expression des dommages, tenant compte des situations accidentelles et du fonctionnement normal, du tribut sanitaire payé par les professionnels et de celui dont souffre le public, le charbon et le pétrole responsables en Europe de centaines de miliiers de décès par an distancent de loin les autres filières ; le nucléaire et les renouvelables sont les bons élèves dans la discipline ; gaz et biomasse ont un niveau de nuisance intermédiaire.
La mortalité par accident, si lourde qu’elle paraisse au moment de l’accident, ne représente qu’une très faible partie, en nombre de morts moins de 0,5 % de la mortalité précoce (différée) due aux sources d’énergie, principalement les combustibles fossiles et le nucléaire, les autres sources d’énergie contribuant peu. C’est donc l’évaluation des mortalités différées qui permet de comparer véritablement la dangerosité des différentes sources.
Par unité d’énergie produite on constate que le nucléaire contribue en fait considérablement moins à cette mortalité différée que ne le font les combustibles fossiles. Une des raisons est qu’il ne peut le faire qu’à l’occasion d’accidents graves entraînant une importante contamination radioactive tandis que les combustibles le font en fait en permanence du simple fait de la pollution atmosphérique qu’entraîne leur utilisation.
Dans les deux cas, cette mortalité différée est évaluée à partir de relations dose effet issues d’études épidémiologiques. Pour une contamination radioactive, la pente de cette relation dose effet est évaluée à 5% par sievert de dose efficace. Pour la pollution atmosphérique, si l’on utilise le marqueur des PM 2,5, cette pente est à peu près de 5 % par 10 µg/m3 de concentration de PM 2,5 dans l’air. Cela signifie que vivre 50 ans dans une atmosphère à 15-20 µg/m3 de PM 2,5 comme c’est le cas dans les grandes villes françaises est à peu près équivalent, du point de vue de la mortalité différée à vivre 50 ans dans une zone contaminée par la radioactivité à 20 mSv par an.
Remerciements : Ce travail a particulièrement bénéficié des contributions de Bernard Durand et André Aurengo de même que de la vigilance et des conseils de Jean Pierre Schwartz, Hervé Nifenecker, Gilbert Ruelle, Frédéris Livet, Henri Prévot et Jean Marie Seiler.
Table des matières
Coût sanitaire de l’énergie. 1
2 - Identification des risques. 2
2-2 Impact en fonctionnement normal. 6
2-2-3 Autres sources d’énergie. 28
2-2-4 Normalisation et comparaison des risques en matière de production d’électricité. 29
[1] Subsidies and costs of EU energy 2014
[2] Hirschberg et al : Severe accidents in the Energy Sector 1st Edition Swiss Federal Office of Energy 1998
[3] Burgher P, Hirschberg S. Comparative risk assessment of severe accidents in the energy sector. Energy Policy, 74, 2014, S45-S56.
[4] Dans ce texte les unités en GWe et TWe.unité de temps font toutes référence à l’énergie produite et non à l’énergie consommée.
[5] Les évacuations de plus de 200 personnes ont résulté de : 65 accidents pour le pétrole, 28 pour le LPG, 18 pour le gaz naturel, 3 pour les barrages, 2 pour le nucléaire. L’ensemble des évacués a affecté plus de 1 million 500.000 résidents. Parmi les évacuations les plus importantes figurent pour le LPG : 220.000 évacués en 1979 à Missisauga Canada et 200.000 en 1984 à Mexico ; pour l’hydroélectricité : 150.000 évacués en 1979 à Moravi en Inde ; pour le nucléaire 144.000 évacués en 1979 aux USA, TMI et 135.000 en 1986 en Ukrraine, Tchernobyl ; pour le pétrole : 100.000 évacués en 1988 à Mexico.
[6] Il existe quelques données concernant les accidents du photovoltaïque en fonction des techniques retenues (Fthenakis et al Solar Energy, 85,1609, 2011), elles concernent une centaine de décès, conduisant à un taux normalisé de l’ordre de 10-3 par GWe.année ; il faut y ajouter les décès imputables à l’installation des panneaux en toiture dont il n’existe pas d’évaluation globale. Il n’existe pas de base de données complète pour l’accidentologie dans la filière éolienne ; en dépit d’accidents matériels divers les accidents humains sont rares. Dans une revue du Los Angeles Times du 3/08/2011, 78 accidents fatals seraient intervenus de 1970 à 2010 dont la moitié aux USA. Dans la filière offshore, 959 accidents ont été répertoriés en 2014 en Europe du Nord justifiant 44 jours d’arrêt de travail, aucun accident fatal n’a été déploré (Environnement et technique 348, 2015). L’inventaire le plus complet apparaît dans les actes du Caithness Windfarm forum 2017 et concerne 2057 accidents et 130 décès dans le monde (http://www.caithnesswindfarms.co.uk/accidents.pdf) mais la statistique pourrait ne couvrir que moins de 10% des accidents réels selon les auteurs.
[7] On ajoute au passif des expositions une part de 0,2% par Sv de risque d’induction de maladies génétiques transmissibles bien qu’aucune donnée épidémiologique n’en ait établi l’existence.
[8] Le nombre de 33.000 décès par cancer est obtenu à partir d’une évaluation de la dose collective mondiale d’environ 600.000 hommes.sievert issue du rapport TORCH 2006 consécutif au forum Tchernobyl. Le coefficient de risque retenu, quelle que soit la dose, est de 5% de cancers fatals par Sv. La révision de 2008 du rapport UNSCEAR aboutit en fait à une dose collective mondiale d’environ 300.000h.Sv qui devrait conduire à une estimation maximale de 15.000 cancers fatals dans l’hypothèse d’une relation de risque linéaire sans seuil.
[9] United Nations Scientific Committee on the effect of Atomic Radiation : Sources and Effects of Ionizing Radiation United Nations 2008
[10] The Japan Times Feb 20 2014
[11] Samet J, Chanson D. Fukushima Daiichi Power Plant Disaster : how many people were affected, 2015 Report
[12] IRSN Methodologie appliquée par l’IRSN pour l’évaluation du coût d’accidents nucléaires en France, PRP-CRI/SESUC/2013-00261 , 2013.
[13] Yablokov et al Chernobyl consequences of the catastrophe…Ann Acad Sci NY 181, 2009
[14] OCDE Electricité nucléaire : Quels coûts externes, NEA 4373, OCDE 2003
[15] Rabl A Spandaro J Les coûts externe de l’électricité, revue de l’énergie, 525, 151, 2001
[16] United Nations Scientific Committee on the effect of Atmic Radiation : Sources and Effects of Ionizing Radiation United Nations 2000
[17] Becker K Health Effects of High Radon Environment Non linearity in biology toxicology and medicine, 1, 3, 2003
[18] Rage E et al Cohorte française des mineurs d’uranium, Archives des maladies professionnelles et de l’environnement, 74,669, 2013
[19] Richardson D et al Risk of cancer from occupational exposure to radiation, doi: 101136/bmj/h5359
[20] Rosental PA. La silicose comme maladie professionnelle transnationale. Revue Française des Affaires Sociales 2008/2 La Documentation Française
[21] Coal workers pneumoconiosis in Germany, HealthGrove global Health Statistics 2017
[22] HSE, Coal workers pneumoconiosisi statistics 2017
[23] Huang Irène in Santé et travail à la mine, Judith Rainhorn, Presse Universitaire le Septentrion, 2014 pages 207-234.
[24] Ref : Bernard Durand communication personnelle.
[25] Pascale M et al : Changement climatique et santé. Bulletin Epidémiologique Hebdomadaire 38-39, 718, 2015
[26] Jacobson M, On the causal link between carbon dioxide and air pollution mortality. Geophysical Research Letters, 35, L03809, 2008
[27] Laden F et al Association of fine particulate matter from different sources with daily mortality in 6 US cities. Environ Health Perspect 108, 941, 2000 ; Thurston G Heart disease mortality and long term exposures to source related components of US fine particle air pollution. EHP, 124, 785, 2016
[28] Pope CA, Health effects of particulate matter air pollution EPA wood smoke webinar, July 28, 2011
[29] Pope CA, Health effects of particulate matter air pollution EPA wood smoke webinar, July 28, 2011
[30] Pope CA et al Fine particle air pollution and life expectancy in the United States, New England Journal of Medicine, 360, 376, 2009.
[31] Hoek et al Long term air pollution and cardio-respiratory mortality. Environmental Health 12, 43, 2013
[32] COMEAP Committee on the medical effects of air polution, The mortality effects of long term exposure to particulate air pollution in the UK, 2010
[33] Santé publique France. Impact de l’exposition chronique aux particules fines 2016
[34] Hamra G et al Outdoor particulate matter exposure and lung cancer: a litterature review and metaanalyse, Environ Health Perspect 122, 906, 2014.
[35] Raaschou-Nielsen O et al Particulate matter air pollution and lung cancer Environ Int 87, 66, 2016
[36] Brook et al Particulate matter air pollution and cardiovascular disease. Circulation, 121, 2331, 2010
[37] Pope et al Exposure to fine particle air pollution is associated with endothelial injury and inflammation Circulation Research, doi: 10.1161/CIRCRESAHA. 116.329279, 2016
[38] 10 mg/m3 pour une exposition de 8 heures.
[39] Revihaap : WHO Review on evidence of health effects of air pollution Report 2013
[40] Dominici F et al Chemical composition of fine particulate and life expectancy Epidemiology 26, 556, 2015
[41] Gauderman W et al The effects of air pollution on lung development N Engl J Med. Sep 9;351(11):1057-67, 2004
[42] Fisher PH et al Air pollution and mortality in seven million adults. Environ Health Perspect 123, 697, 2015
[43] Hamra G et al Lung cancer and exposure to nitrogen dioxide and traffic. Environ Health Perspect 123, 1107, 2015
[44] Revihaap : WHO Review on evidence of health effects of air pollution Report 2013
[45] Atkinson R et al ; Long term exposure toambient ozone and mortality. BMJ open 2016 6:e009493
[46] Brook et al Particulate matter air pollution and cardiovascular disease. Circulation, 121, 2331, 2010
[47] Pope et al Exposure to fine particle air pollution is associated with endothelial injury and inflammation Circulation Research, doi: 10.1161/CIRCRESAHA. 116.329279
[48] Revihaap : WHO Review on evidence of health effects of air pollution Report 2013
[49] Lippman M Chen L. Health effects of concentrated ambient particulate air matter and its components. Critical review in toxicology 39, 865, 2009
[50] Raaschou-Nielsen O et al. Particulate matter air pollution components and risk for lung cancer. Environ Int. 87, 66, 2016.
[51] Laden F et al Association of fine particulate matter from different sources with daily mortality in 6 US cities. Environ Health Perspect 108, 941, 2000.
[52] Thurston G Heart disease mortality and long term exposures to source related components of US fine particle air pollution. EHP, 124, 785, 2016
[53] Zu K. et al Long range fine particulate matter from the 2002 Quebec forest fires and daily mortality in Greater Boston and New-York city. Air Qual Atmos Health, 9, 213, 2016
[54] Nasari M; et al. A class of non linear exposure response models suitable for health impact assessment applicable to large cohort studies of ambient air pollution. Air Qual Atmos Health, 9, 961, 2016.
[55] Brook et al Particulate matter air pollution and cardiovascular disease. Circulation, 121, 2331, 2010
[56]Pope CA, Health effects of particulate matter air pollution EPA wood smoke webinar, July 28, 2011
[57] Synthèse dans Hidden costs of Energy : unpriced consequences of energy production and use. National Academy of Science 2009
[58] Externe Externalities of Energy,Methodology Update EUR 21951, 2005
[59] ExternE-Pol Final technical Report, Rabl A Spandaro J coordinators, 2nd version Aug 2005
[60] Externe Externalities of Energy,Methodology Update EUR 21951, 2005
[61] Dans le cas de l’ozone aucune donnée n’est disponible au-dessous de 100µg/m3 et l’OMS recommande de ne considérer que les périodes d’exposition au-dessus de 70µg/m3 (35ppb).
[62] Santé Publique France. Impacts de l’exposition chronique aux particules fines sur la mortalité en France continentale et analyse des gains de santé de plusieurs scenarios de réduction de la pollution atmosphérique. 2016
[63] Leksell I Rabl A. Air pollution and mortality : quantification and valuation of years of life lost. Risk Analysis, 21, 843, 2001
[64] NewExt New Elements for the Assessment of External Costs from Energy Technologies. Friedrich R coordinator Final Report Sept 2004
[65] Europe’s Dark Cloud How coal burning countries are making their neighbours sick. 2016
[66] Schmidt JH et al Health effects related to wind turbine noise exposure: a systematic review.PLOS One, doi: 10.1371/journal.pone.01114183
[67] Berger M et al. Health based audible noise guidelines account for infrasound…Frontiers in Public Health. Doi: 10.389/pubh.2015
[68] ANSES Evaluation des effets sanitaires des basses fréquences sonores et infrasons dus aux parcs éoliens. Mars 2017
[69] Rabl A Spandaro J Les coûts externe de l’électricité, revue de l’énergie, 525, 151, 2001
[70] Starfelt N Wikdahl CE Energy forum, Economic analysis of various options in electricity generation taking into account health and environmental effects. Proceedings of Ecological Aspects of Electric Power Generation Wasaw, Nov 14, 2001
[71] Markandya A Wilkinson P. Electricity Generation and Health. The Lancet, 370, 979, 2007
[72] WHO Ambiant air pollution : a global assessment of exposure and burden of disease. WHO 2014